amerikalı patoloq Doroti H. Andersen tərəfindən təsvir edilmişdir, 1901-1964; sinonimləri - qlikogenoz, IV tip, amilopektinoz) - müxtəlif orqanlarda, toxumalarda, əzələlərdə, hüceyrələrdə atipik zəif həll olunan qlikogenin toplanmasına səbəb olan 1,4-alfa-qlükan-şaxələnən fermentin olmaması səbəbindən saxlama xəstəlikləri sinfindən nadir irsi xəstəlikdir. Əsas klinik təzahürlər: həyatın ilk illərində hepatosplenomeqaliya, qaraciyər sirozunun inkişafı ilə mütərəqqi portal fibroz, assit, özofagus varikozları, qaraciyər çatışmazlığı; əzələ hipotenziyası; miyokardın zədələnməsi və ürək çatışmazlığı. Diaqnoz qaraciyərdə, əzələlərdə və s.-də 1,4-alfa-qlükan-şaxələnən fermentin fəaliyyətinin araşdırılması ilə aydınlaşdırılır.İrsiyyət növü autosomal resessivdir. Müalicə simptomatikdir, qlükokortikoidlərin istifadəsi müvəqqəti remissiyanın başlamasına kömək edə bilər. Xəstəliyin proqnozu zəifdir, ölüm uşaqlıqda baş verir, adətən qaraciyər çatışmazlığı səbəbindən.
D. H. Andersen. Anormal glikogenin saxlanması ilə ailəvi qaraciyər sirozu. Laboratoriya Araşdırması, Baltimor, 1956; 5:11–20.
ANDERSEN SİNDROMU
Danimarka həkimi E. D. Andersen tərəfindən təsvir edilmişdir) nadir irsi xəstəlikdir: uzun Q-T intervalı, mədəcik ekstrasistoliyası, əzələ hipotenziyası; kraniofasiyal xüsusiyyətlər xarakterikdir - makrosefaliya (kəllə ölçüsünün yaş normasının 10% -dən çox artması), dolichocephaly (sagittal tikişin vaxtından əvvəl ossifikasiyası səbəbindən kəllə sümüyünün ön-arxa istiqamətdə uzanması), skafosefali (uzun baş qaldırma və boşalma ilə). aşmış qayığın lingi), alçaq qulaqcıqlar, hipertelorizm (geniş məsafəli gözlər), mikroqnatiya (yuxarı çənənin kiçik ölçüsü), braxidaktili (qısa barmaqlı), V barmaqların klinodaktiliiyası (yan və ya medial əyrilik). Varislik növü otosomal dominantdır. Bildirilən halların əksəriyyəti sporadikdir. Müalicə simptomatikdir.
E. D. Andersen, P. A. Krasilnikoff, H. Overad. Fasiləvi əzələ zəifliyi, ekstrasistollar və çoxsaylı inkişaf anomaliyaları: yeni sindrom? Acta peediatrica Scandinavica, Stokholm, 1971; 60:559–564.
13. Priori S. G., Napolitano C., Grillo M. Gizli aritmogen sindromlar: İdiopatik ventrikulyar fibrilasiyanın gizli substratı? // Ürək-damar. Res. - 2001. - Cild. 50.
14. Priori S. G., Napolitano C., Memmi M. Katexolaminergik polimorfik mədəcik taxikardiyası olan xəstələrin klinik və molekulyar xarakteristikası // Sirkulyasiya. - 2002.
Cild. 106. - S. 69-74.
15. Priori S. G., Napolitano C., Tiso N. et al. Ürək rianodin reseptor genindəki mutasiyalar (hRyR2) katexolaminergik polimorfik mədəcik taxikardiyasının əsasını təşkil edir // Yenə orada.
2000. - Cild. 103. - S. 196-200.
16. Spurgeon D. Gənc amerikalılarda qəfil ürək ölümləri 10% artır // Brit. Med. J. - 2001. - Cild. 322.-Səh.573 (Anastrakt).
17. Sumitomo N., Harada K., Naqashima M. et al. Katexolaminergik polimorfik mədəcik taxikardiyası:
© S. M. KRUPYANKO, T. T. KAKUCHAYA, 2005 UDC 616.12-008.6
ANDERSEN SİNDROMU
S. M. Krupyanko, T. T. Kakuçaya
Ürək-damar Cərrahiyyəsi Elmi Mərkəzi. A.
RAMS, Moskva
Andersen sindromu əzələlərin keçici iflici, QT intervalının uzanması ilə xarakterizə olunan nadir irsi patologiyadır, tez-tez yüksək amplitudalı U dalğalarının görünüşü, mədəcik aritmiyaları və dismorfogenez əlamətləri ilə birləşir - aşağı qurulmuş qulaqlar, mikroqnatiyalar (xüsusilə aşağı çənələr, çənənin anormal çənələri), bir və ya bir neçə barmağın forması), sindaktiliya (ayaq və ya əlin ayaq barmaqları arasında birləşmə və ya toxumanın olması), hipertelorizm (iki qoşalaşmış orqan arasında məsafənin artması), qısa boy, skolioz və s. 1971-ci ildə E. Andersen et al. qısa boylu, hipertelorizmi (geniş aralıqlı gözlər), hipoplastik çənələr, geniş burun əsası, yumşaq və sərt damağın bağlanmaması, skafosefalik kəllə (sümükləşmiş sagittal tikiş boyunca silsilə ilə uzun, dar kəllə) və sümüyünün çənəsi olan 8 yaşlı xəstəni bildirdi. 1994-cü ildə R. Tawil et al. 1971-ci ildə Andersen tərəfindən müşahidə edilən kalium-həssas siklik iflic, mədəcik aritmiyaları və dismorfogenez əlamətləri: üç xarakterik əlaməti (klinik triada) olan klinik vəziyyəti təsvir etmək üçün ilk dəfə "Andersen sindromu" terminindən istifadə etmişdir. "Andersen-Tawil sindromu"nun tərifi (Andersen-Tawil sindromu
Qəfil ölümün qarşısını almaq üçün elektrokardioqrafik xüsusiyyətlər və optimal terapevtik strategiyalar // Ürək. - 2003.
Cild. 89, No 1. - S. 66-70.
18. Swan H, Laitinen P. J., Kontula K. et al. Kalsium kanalı antaqonizmi, RYR2 mutasiyaları olan katexolaminergik polimorfik mədəcik taxikardiyalı xəstələrdə məşqlə bağlı mədəcik aritmiyalarını azaldır // J. Kardiovasc. Elektrofiziol. - 2005. - Cild. 16, No 2. - S. 162-166 (Avtomatik).
19. Swan H., Piippo K., Viitasalo M. et al. 1q42-q43 xromosomuna uyğunlaşdırılmış aritmik pozğunluq struktur olaraq normal ürəklərdə bədxassəli polimorfik mədəcik taxikardiyasına səbəb olur // J. Amer. Col. kardiol. - 1999. - Cild. 34, № 7.
20. Tan H. L., Hofman N., Van Langen I. M. və b. Qəfil izah olunmayan ölüm. Sağ qalan qohumlarda kardioloji və genetik müayinənin irsiyyəti və diaqnostik nəticəsi // Dövr. - 2005. - Cild. 112. - S. 207-213.
N. Bakuleva (dirijor - Rusiya Tibb Elmləri Akademiyasının akademiki L. A. Bokeriya)
drome, qısaldılmış ATS). Bu sindromu glikogenozlarla - qlikogen saxlama xəstəlikləri ilə əlaqəli olan Andersen xəstəliyi ilə qarışdırmaq olmaz (qlikogeni çevirən fermentin çatışmazlığı səbəbindən qaraciyərdə, əzələlərdə və digər toxumalarda anormal miqdarda qlikogen toplanır). Andersen sindromu kanalopatiyalar - ion kanal patologiyaları bölməsində təsvir edilən ilk patologiya idi. Andersen sindromu otosomal dominant şəkildə miras alınır, baxmayaraq ki, sporadik hallar haqqında məlumatlar var. Onun miras yolu ilə ötürülmə ehtimalı 50%-dən çoxdur. Xəstəliyin şiddəti eyni ailə daxilində dəyişə bilər - bir uşaqda ciddi bir zədə ola bilər, digərində isə klinik olaraq asemptomatik ola bilər. Xəstəliyin penetranlığı çox dəyişkəndir və bütün xəstələr bu sindromun bütün klinik xüsusiyyətlərini göstərmir. Ritm pozğunluqları xəstənin qan zərdabında kalium səviyyəsində kəskin dalğalanmalar səbəbindən ikinci dəfə yaranan əzələ iflicinin hər hansı bir hücumunu müşayiət edir (Şəkil 1). Bununla belə, ədəbiyyatda ritm pozğunluqlarının Andersen sindromunun ilk klinik təzahürü olduğu və əzələ parezi və iflicinin epizodlarından əvvəlki hallar təsvir edilmişdir. Bu xəstəlik fenotipi ilə daha sonra QT intervalının uzadılması müəyyən edilmişdir. Andersen sindromunda qəfil ürək ölümü halları da bildirilmişdir.
ARHİTMOLOGİYA SALNALARI, №4, 2005-ci il
ARHİTMOLOGİYA SALNALARI, №4, 2005-ci il
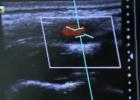
III AVF V3 * V6 Serum K+=2.9
III AVF V3 V6 Serum K+=3.4
düyü. 1. Hipokalemiya (a) fonunda Andersen sindromlu 16 yaşlı qızda mədəciklərin bigeminiya epizodu (ulduz işarələri mədəcik ekstrasistollarını göstərir); b - qanda kalium səviyyəsinin normallaşması aritmiyanın yox olmasına səbəb oldu.
Serum K+ - serum kalium.
Əhali arasında yayılmanın az olmasına baxmayaraq, Andersen sindromu müasir tibb üçün böyük elmi və praktiki maraq doğurur, çünki bütün genetik cəhətdən müəyyən edilmiş kanalopatiyalar arasında həm zolaqlı (skelet) əzələləri, həm də ürək əzələlərini təsir edən yeganə xəstəlikdir. Əzələ parezi və iflici ilə təzahür edən digər xəstəliklər skelet əzələ hüceyrələrində natrium, kalsium və kalium ionlarının daşınmasına cavabdeh olan genlərdəki mutasiyalar, uzun QT sindromunun müxtəlif formaları isə yalnız kardiomiositlərdə natrium və kalium ionlarının daşınmasını kodlayan genlərin mutasiyaları nəticəsində yaranır. Əvvəlki tədqiqatlar Andersen sindromunun allel genezisi ehtimalını istisna edirdi. Bununla belə, 2001-ci ildə N. Plaster et al. böyük bir ailədə (15 nəfər) molekulyar genetik tədqiqat apararkən, Andersen sindromunun irsiyyət ehtimalı ilə 23-cü xromosomun 17q lokusunun patologiyası arasında əlaqə aşkar edildi və KCNJ2 geninin heterozigotlu yanlış mutasiyasını aşkar etdi (xromosomun 17q lokusunun KCNJ2N - lokusunun 17q lokusunun 23-cü xromosomu ilə). 3.1-17q24.2) . Andersen sindromu olan xəstələrin 50%-dən çoxunda KCNJ2 genində mutasiyalar aşkar edilmişdir ki, bu da KCNJ2 geninin bu patologiyanın inkişafına cavabdeh olduğunu təsdiqləyir. Hal-hazırda, Andersen sindromuna səbəb olan KCNJ2 geninin 20-dən çox heterozigot yanlış sens mutasiyaları müəyyən edilmişdir (Şəkil 2). KCNJ ailəsinin genləri müxtəlif toxumalarda geniş şəkildə ifadə olunur: əzələlər (KCNJ2, KCNJ11), ürək (KCNJ2, KCNJ3, KCNJ5, KCNJ11), beyin (KCNJ3, KCNJ6, KCNJ9, KCNJ11), epitel (KCNJ11), epitel (KCNJ11) və başqaları. KCNJ gen ailəsindəki mutasiyalar insanlarda üç irsi xəstəliyin, siçanlarda isə bir xəstəliyin inkişafına səbəb ola bilər. Beləliklə, KCNJ1 genindəki mutasiyalar (Kir1.1) hipokalemiya və insan orqanizmi tərəfindən natrium itkisi ilə xarakterizə olunan otosomal resessiv xəstəlik olan Bart-ter sindromunun inkişafına səbəb olur; KCNJ11 (Kir6.2) genindəki mutasiyalar və onunla əlaqəli SUR1 zülalları daimi hiperinsulinemiyanın inkişafına səbəb olur.
düyü. 2. Kir2.1 kanalının alt bölməsinin strukturu.
Məsamə - mərkəzi çuxur (məsamə); M1, M2 - transmembran domenləri; hüceyrədənkənar - hüceyrədənkənar; hüceyrədaxili - hüceyrədaxili.
Boz qutular hazırda Andersen sindromu olan xəstələrdə müəyyən edilmiş 20 mutasiyanı göstərir; ağ qutu qısa QT sindromunda müəyyən edilmiş mutasiyanı göstərir.
uşaqlarda qlikemiya, Kir3.2 (GIRK2) mutasiyalar - neyronların itirilməsi və ağır ataksiya ilə özünü göstərən siçanlarda autosomal resessiv patologiyaya və nəhayət, KCNJ2 genindəki mutasiyalar Andersen sindromunun inkişafı ilə əlaqələndirilir. KCNJ2, kardiyomiyositlər, zolaqlı əzələ hüceyrələri və beyin də daxil olmaqla, həyəcanlanma qabiliyyətinə malik hüceyrələrdə kalium kanalının bir hissəsi olan Kir2.1 zülalının sintezini kodlaşdırır. Kir2.1 kanalları ürək və skelet əzələlərinin istirahət membran potensialının və beləliklə, bütövlükdə bu toxumaların hüceyrələrinin həyəcanlılığının ən vacib tənzimləyiciləridir, çünki onlar fəaliyyət potensialının repolarizasiyasının son mərhələsində hiperpolyarlaşdırılmış membrana malik hüceyrələrdən kalium ionlarının buraxılmasını təmin edir. Kir2.1 zülalı iki transmembran domeni (M1, M2) və mərkəzi açılış (məsamə) (H5) olan 427 amin turşusundan ibarətdir və repolarizasiya mərhələsinin gecikmiş düzəldilməsi ilə kalium cərəyanının IK1 komponentini tənzimləyir (bax. Şəkil 2). Northern blot analizi ürək, beyin, plasenta, ağciyərlər və skelet əzələlərində yüksək miqdarda Kir2.1 olan KCNJ2 geninin 5,5 KB transkripsiyasını və böyrəklərdə daha az məzmunu aşkar etdi. Ürəkdə Kir2.1 kanalları qulaqcıqlarda, mədəciklərdə (IK1 cərəyanının yüksək keçiriciliyi ilə) və Purkinje liflərində üstünlük təşkil edir və nodal hüceyrələrdə daha az rast gəlinir. KCNJ2 geni ilə kodlanan Kir2.1 alt bölmələri kardiyomiyositlərin hüceyrə divarının içərisində tetramerə birləşərək fəaliyyət göstərən kanal əmələ gətirir; onlar həmçinin Kir2.1 ailəsinin digər alt bölmələri ilə heteromultimerlər kimi birləşə bilər ki, bu da onların funksional mürəkkəbliyini və müxtəlifliyini göstərir. KCNJ2 genindəki mutasiyaların əksəriyyəti səhv mutasiyalardır.
IK1 cərəyanının azalmasına, repolarizasiyanın azalmasına və fəaliyyət potensialının müddətinin artmasına səbəb olan dominant-mənfi təsirə malikdir. Yuxarıda göstərilən proseslər nəticəsində ventrikulyar aritmiyaların və ya skelet əzələlərinin miotonik daralmalarının görünüşünü başlatan istirahət membran potensialının depolarizasiyası və destabilizasiyası baş verir. Bundan əlavə, tədqiqatçılar Kir2.1 kanalının disfunksiyası və IK1 cərəyanının azalmasının qeyri-həyəcanlı toxumalarda siqnal disfunksiyalarının inkişafında mühüm rol oynadığını, Andersen sindromu olan xəstələrdə dismorfogenezin təzahürlərini izah edə biləcəyini təklif edirlər. M. Tristani-Firouzi və b. dəyişdirilmiş proteinin in vitro ifadəsi ilə Andersen sindromunda mutasiyaların funksional nəticələrini öyrənmişdir. Bu günə qədər müəyyən edilmiş bütün növ mutasiyalarda Kir2.1 kanalının funksiyasının əhəmiyyətli dərəcədə pisləşməsi müşahidə edilmişdir.
Andersen sindromunun klinik təzahürləri son dərəcə dəyişkəndir, bu, xəstəliyin müxtəlif fenotiplərinin təzahürünə kömək edən müxtəlif mutasiyaların olması ilə izah olunur. Çox güman ki, digər ion kanallarında olan qüsurlar da Andersen sindromunun etiologiyasında əhəmiyyətlidir. Dövri olaraq meydana gələn əzələ iflici miyositlərin kalsium, natrium və kalium kanallarının patologiyası ilə bağlı ola bilər. Xəstələr qollarda, ayaqlarda, ümumiləşdirilmiş parezi və əzaların iflicinə qədər qısamüddətli zəiflik epizodlarını hiss edirlər. Belə hücumlar istirahətdə, fiziki gücdən sonra və ya səhər oyandıqda müşahidə edilə bilər. Qeyd etmək lazımdır ki, xəstəliyin tetikleyici faktorları müxtəlifdir. Hal-hazırda, Andersen sindromunda əzələ iflici hücumunun başlamasına səbəb olan bütün qida amilləri məlum deyil. Ehtimal ki, kalium və qlükoza ilə zəngin qidalar tetikleyicilərə aid edilə bilər. Dövri əzələ iflicinin meydana gəlməsinə səbəb olan digər amillər ola bilər: fəaliyyətlərdə dəyişiklik - fiziki gücdən sonra istirahət, uzun oturmadan sonra fiziki fəaliyyət, yuxudan sonra oyanmaq, boş bir mədədə uzun gəzinti, doyurucu yemək. İstənilən soyuqdəymə də əzələ iflicinə səbəb ola bilər; ədəbiyyatda tetikleyicilərin inhalyasiya edilmiş qazlar - karbon qazı, benzin buxarları və ya hətta yağlı boya qoxusu olduğu hallar barədə məlumatlar var. Tristani-Firuozi tədqiqatında KCNJ2 gen mutasiyaları olan 36 xəstənin 23-də (64%) siklik əzələ iflici müşahidə olunub. Fiziki gərginlikdən sonra istirahət, oxşarların klassik variantlarında olduğu kimi, əzələ iflicinin baş verməsində ən çox yayılmış tətik idi.
xəstələrin əksəriyyətində (55%) hipokalemiya (zərdabda kaliumun konsentrasiyası 3,4 mEq / l-dən az və ya bərabər) olduğu halda, hiperkalemiya 22%, normokalemiya isə xəstələrin 10% -də müşahidə edilmişdir. Bununla belə, Andersen sindromunda hipokalemik vəziyyətlər, hipokalemik əzələ iflicinin klassik variantlarında olduğu kimi, karbohidratların qəbulundan əvvəl deyildi. 12 xəstədə aparılan əzələ biopsiyası qeyri-spesifik dəyişiklikləri - siklik əzələ parezi və ya iflicinin digər formalarında müşahidə olunan kiçik miopatiyalar və/yaxud boru aqreqatları aşkar edib. Karbon anhidraz inhibitorları Andersen sindromunda, eləcə də əzələ iflicinin klassik formalarında iflic hücumlarının tezliyini azaltmaqda təsirli olmuşdur.
Andersen sindromlu xəstələrdə EKQ-də ən xarakterik dəyişikliklər OT intervalının uzanması və yüksək amplitudalı dalğalardır və (şək. 3). Hazırda uzun OT interval sindromunun variantlarından birində Andersen sindromunun iştirakı ilə bağlı tədqiqatçılar arasında ziddiyyətli fikirlər mövcuddur. Andersen sindromu əzələ hüceyrələrinin repolarizasiyasının genetik olaraq müəyyən edilmiş patologiyası hesab edildiyi üçün uzun QT sindromu (ST), yəni tip 7 (HOTT) adlandırılmağa başlandı. Hazırda uzun QI sindromunun tipik klinik təzahürlərinin inkişafı üçün etibarlı cavabdeh olan mutasiyalar 5 gen müəyyən edilmişdir: KSIO1 (ST1), SNAO (XSN2, BT2), SSN5L (ST3), KSOE1 (ST5), KSOE2 (ST6). Anadangəlmə uzun WC sindromunun digər formalarına bənzər, yan tərəfdə əsas təzahürdür
düyü. 3. Andersen sindromu olan xəstələrdə aşkar edilən ən tipik elektrokardioqrafik dəyişikliklər və ritm pozğunluqları. a - OT intervalının uzadılması; b - mədəcik bigeminy izlədi qeyri-sabit polimorf mədəcik taxikardiya qısa run; c - iki istiqamətli ventriküler taxikardiya; d - oxlar çıxan dişləri göstərir və.
ARHİTMOLOGİYA SALNALARI, №4, 2005-ci il
ARHİTMOLOGİYA SALNALARI, №4, 2005-ci il
Andersen sindromunda ürək-damar sistemi KSSh2 geninin bütün daşıyıcılarının 71% -ində müəyyən edilmiş OT intervalının uzanması idi. Andersen sindromu olan kişi və qadın probandlarda düzəldilmiş OT intervalının (OTS) orta dəyəri müvafiq olaraq 479 və 493 ms, uzunmüddətli OT sindromunun digər formalarında isə müvafiq olaraq 497 və 510 ms təşkil etmişdir. Uzadılmış OT intervalının olması və həyati təhlükəsi olan ventriküler aritmiyaların inkişaf ehtimalı səbəbindən bəzi tədqiqatçılar Andersen sindromunu anadangəlmə uzadılmış OT sindromunun alt növlərindən biri hesab edirlər. Lakin, məlum olduğu kimi, mədəcik aritmiyalarının tez-tez baş verməsinə baxmayaraq (ventriküler ekstrasistoliyalar və qeyri-sabit mədəcik taxikardiyalarının, o cümlədən iki istiqamətli mədəcik taxikardiyalarının Şəkil 3-ə baxın) - M. 118111110-da qəfil ölüm riski olan xəstələrin 64% -ində ani ölüm riski aşağı idi. uzun interval sindromu OT və digər irsi kanalopatiyalarda. Andersen sindromunda mədəcik aritmiyalarının baş vermə mexanizmlərini aşkar etmək üçün müəlliflər təcrübədə mədəcik kardiyomiyositlərinin Jr2.1 kanalının funksiyasının boğulmasını simulyasiya etmişlər. Məlum olub ki, hipokaliemiya fonunda Jr2.1 kanal funksiyasının boğulması ürək əzələsinin fəaliyyət potensialının son fazasının uzanmasına, Na+/Ca2+ mübadiləsinin induksiyası ilə əlaqədar gecikmiş postdepolyarizasiyaların baş verməsinə və spontan aritmiyaların inkişafına səbəb olub. Müəlliflər bu qənaətə gəliblər
Andersen sindromunda mədəcik aritmiyalarının baş verməsi üçün substratın anadangəlmə uzun WATS-in digər formalarından fərqli olduğunu və Ca2+ həddindən artıq yüklənməsi və ya rəqəmsal intoksikasiya (məsələn, iki istiqamətli və polimorfik mədəcik taxikardiyası kimi) nəticəsində yaranan aritmiyalara daha çox oxşar olduğunu. Beləliklə, Andersen sindromunda anadangəlmə uzun OT interval sindromu və ailəvi (katekolaminerjik) polimorf mədəcik taxikardiyasının klinik təzahürləri birləşdirilir (sonuncu ilə, bir qayda olaraq, uzadılmış OT intervalı müşahidə edilmir). Andersen sindromunda baş verən aritmiyaların spektri cədvəldə təqdim olunur.
Dişlərin yüksək amplitudası Andersen sindromunda xüsusi bir tapıntıdır və əsasən anterior sinə keçiricilərində qeydə alınır (bax. Şəkil 3). Bu xüsusiyyət M.linstom-Toru21-ə görə probandların 76% və mutant KSS2 genlərinin daşıyıcılarının 47% -ində aşkar edilmişdir. Qeyd etmək lazımdır ki, normal olaraq sağlam insanlarda dalğa və nadir ürək ritmi ilə qeydə alına bilər, M. linstom-Igou21 tədqiqatında Andersen sindromu olan probandlarda isə orta ürək dərəcəsi 84 ± 17 döyüntü / dəq (52-dən 115 döyüntü / dəq) idi. Məlumdur ki, hipokalemiyada və dalğanın amplitudası da yüksək ola bilər, lakin biz yüksək amplitudalı dişləri olan xəstələrdə qan zərdabında kaliumun səviyyəsini əks etdirən əsərlər tapa bilmədik, buna görə də yüksək amplitudalı dişlərin yaranmasında və Andersen sindromunda hipokalemiyanın rolunu istisna etmək olmaz. Avto-
Mutant KSNP geni olan probandlarda Andersen sindromunun klinik təzahürləri
Mutasiya Klasteri Cins HR Müddəti OT, ms Ritm pozğunluqları
D71V 4415 F 100 513 Tapılmadı
A95-98 (A-deletion) 3328 F 83 475 Bigeminia, polimorfik VT
8136B 6634 F 68 500 Bigeminia
P186b 7246 M 94 PBBNPG* Polimorfik VT
R218W 2401 F 100 560 Bigeminy, ölümcül olmayan ürək dayanması, 1-ci dərəcəli AV blok, titrəmə, mədəciklərin çırpınması
R218W 2679 M 68 510 Bigeminia, polimorfik VT
R218W 2681 F 75 488 Bigeminy polimorfik VT
R218W 7480 M 94 525 Bigeminia
R218W 6515 M 52 416 Bigeminia, polimorfik VT
R218Q 6562 M 70 469 Aşkarlanmadı
G300V 3677 F 100 480 Bigeminy polimorfik VT
V302M 2682 M 79 PBPNPG* Bigeminia
E303K 2281 F 85 495 Tez-tez mədəcik ekstrasistolları
A314-315 5768 F 115 471 Flicker, mədəciklərin çırpınması, monomorfik VT
* Sağ budaq blokunun tam blokadası OT intervalının dəqiq ölçülməsinə mane oldu.
Biz həmçinin mutasiyaların şiddəti (Kr2.1 kanal disfunksiyasının şiddəti) ilə Andersen sindromunun klinik təzahürlərinin şiddəti (OTS-nin uzanması, aritmiya, sinir-əzələ simptomları, dismorfogenez) arasındakı əlaqəni qiymətləndirdik. Məlum oldu ki, xəstəliyin kliniki fenotipi K1r2.1 kanal funksiyasının dominant-mənfi supressiya dərəcəsi ilə uyğun gəlmir.
G. Andelfinge və başqaları. 41 qan qohumunda KSSh2 geninin R67W heterozigotlu missens mutasiyasını müəyyən etdikdə, mədəcik aritmiyalarının və dövri əzələ iflicinin irsiyyətinin cinsə görə fərqləndiyi məlum oldu: beləliklə, mədəcik aritmiyaları qadınlarda (13-də 16-da) və ya kişilərdə (15-dən 15-də) və ya kişilərdə üstünlük təşkil edirdi. 40%). Eyni zamanda, mədəcik aritmiyaları 10 yaşından sonra görünməyə başladı və hamiləlik dövründə (qadınlarda KSH2 gen mutasiyalarının digər növləri ilə hamiləlik dövründə ritm pozğunluqları daha tez-tez müşahidə edildi) və 55 yaşdan sonra (menopoz zamanı) daha az müşahidə edildi. Maraqlıdır ki, bu damazlıqda OT intervalının uzadılması müşahidə edilməmişdir. Bu qrup xəstələrdə üçdə tarixdə bayılma müşahidə edildi; qəfil ürək ölümündən sağ çıxan bir xəstə implantasiya edilmiş kardioverter defibrilator aldı. 8 kişi xəstədə fiziki gücdən sonra əzələ zəifliyi və ya iflic epizodları, 2 xəstədə hipokaliemiya qeyd edildi. 4 nəfərdə hipertelorizm, 10 nəfərdə kiçik alt çənə, 9 nəfərdə əl və ya ayaq barmaqlarının sindaktiliyası, 12 nəfərdə klinodaktiliya müşahidə olunub. Dismorfogenez əlamətləri kişilərdə və qadınlarda eyni dərəcədə geniş yayılmışdır. Skoliozun cərrahi müalicəsi 1 kişi xəstəyə, damağın tıkanmamasına görə isə 1 qadın xəstəyə aparılmışdır. Tədqiq edilmiş şəcərədə birtərəfli böyrək displaziyasının və ürəyin qapaq patologiyasının - ağciyər qapağının stenozu (bir xəstədə 6 aylıq yaşda diaqnoz qoyulmuş), ikibucaqlı aorta qapağı (3 xəstədə) və aorta koarktasiyası olan ikiüzlü aorta qapağının (1 xəstədə) aşkarlanması çox qeyri-adi olmuşdur. Belə anormallıqlar ilk dəfə Andersen sindromu olan xəstələrdə müəyyən edilmişdir. Bundan başqa, yeni doğulan körpənin ürək qüsuru ilə ölüm xəbəri də yayılıb. Atrioventrikulyar (AV) I dərəcəli blokada 4 kişi və bir qadında sol budaq blokunun blokadası ilə birlikdə müşahidə edildi. Heç bir fərd eyni zamanda Andersen sindromuna xas olan bütün təzahürlərə malik deyildi. İçərisində Andersen sindromunda fenotipik təzahürlərin pleiotropiyası
Bu damazlıq (şək. 4) ya R67W mutasiyasının spesifik təsiri, ya da allellərin ifadəsinin dəyişməsi, ya da xarici amillərin dəyişdirici təsiri ilə izah edilə bilər.
Andersen sindromu üçün istifadə edilən müalicənin bir neçə təsviri var. Nümunə olaraq J. Junker və başqalarının mesajını nəzərdən keçirək. : ailə tarixi olmayan 6 yaşlı qadın xəstədə ilk dəfə irsi və ürək-damar xəstəlikləri ilə ağırlaşan atonik parezlərin təkrarlanan epizodları yaşanmağa başladı. 10 yaşında o, EKQ-də qeydə alınmış asemptomatik polimorf mədəcik ekstrasistolları (PV) və zərdabda kreatinin-burun səviyyəsinin yüksək olması (447 U/L-ə qədər) səbəbindən poststreptokokk miokarditdən şübhələnirdi. Əzələ zəifliyinin kortəbii dayandırılması səbəbindən həkimlər onların psixogen mənşəli olma ehtimalını istisna etmədilər. 15 yaşında xəstə mədəcik fibrilasiyası (VF) epizodunu yaşadı və ürək-ağciyər reanimasiyası uğurla həyata keçirildi. Proqramlaşdırılmış elektrik stimullaşdırılması ilə davamlı mədəcik taxikardiyaları yarandı, QTc 0,45 s idi. Xəstəyə kardioverter defibrilator (ICD) implantasiya edilib. Bir il sonra ICD şokları tələb edən VF-nin gündəlik hücumları baş verməyə başladı və şiddətli əzələ zəifliyi (əzələ iflicinə qədər) epizodları müşahidə edildi. Fiziki müayinə zamanı xüsusiyyətlərdən aşağıdakılar diqqəti cəlb etdi: geniş burun bazası, klinodaktiliya, skolioz və qısa boy. Atonik əzələ iflici yuxarı və aşağı ətrafların müxtəlif əzələ qruplarını əhatə edir, qəfil baş verir, bir neçə saat və ya gün davam edir və öz-özünə dayanır. Serum kalium və kreatin kinaz səviyyələri normal idi. Zəiflik hücumları hiperkalemiya və ya soyuqdəymə nəticəsində yarandı və məşq əzələ fəaliyyət potensialının azalması ilə müşayiət olundu. Əzələ biopsiyası boruşəkilli aqreqatlar və bir neçə vakuol aşkar etdi. Andersen sindromunun sporadik variantının kliniki diaqnozu qızda KCNJ2 geninin R218W heterozigotlu missens mutasiyasını aşkar edən molekulyar genetik tədqiqatdan sonra təsdiqlənib, lakin onun valideynlərində deyil. Sotalol və I sinif antiaritmik dərmanlar (AARPs), o cümlədən flekainid və propafenon təsirsiz idi. Amiodaron gündə 200 mq yükləmə dozasında kaptopril, nadolol və digitoxin ilə terapiyaya əlavə edildi. Ventriküler aritmiya tez bir zamanda yox oldu və əzələ zəifliyi hücumları təkrarlanmağa davam etdi. 2 aydan sonra yuxarıda göstərilən terapiyaya gündə 750 mq dozada asetazolamid (diamox) əlavə edildi. Növbəti 2 il ərzində xəstə
ARHİTMOLOGİYA SALNALARI, №4, 2005-ci il
ARHİTMOLOGİYA SALNALARI, №4, 2005-ci il
1 Andersen sindromu olan xəstələrdə amiodaron və asetazolamid terapiyasının uğursuzluğu və ya yan təsirlərin inkişafı səbəbindən onu dayandırmaq zərurəti haqqında məlumat verir. Digər tərəfdən, R218W tipli mutasiya ilə amiodarona və asetazolamidə terapevtik cavab arasında farmakogenetik qarşılıqlı əlaqə ola bilər ki, bu da digər xəstələrdə təsdiq edilməlidir. Amiodaron IK1 cərəyanını maneə törətdiyindən, natrium və kalsium kanallarının, həmçinin beta-adrenergik reseptorların fəaliyyətini yavaşlatmaqla ürək əzələsinin hiper həyəcanlılığını maneə törətdiyini güman etmək məntiqlidir.
xəndək, bununla da South2.1 kanalının funksiyasını itirməsi nəticəsində yaranan dəyişiklikləri düzəldir. Bununla belə, əhəmiyyətli əlavə təsirlər potensialına görə, amiodaron simptomatik aritmiyaları olan xəstələrə tövsiyə edilə bilər. Qanın turşuluğunu dəyişdirən bir dərman olan asetazolamid, əzələ Ksa2+ kanallarının seçmə açılması səbəbindən istənilən mənşəli əzələlərin dövri iflicinin qarşısını ala bilər ki, bu da IK1 cərəyanının disfunksiyasını kompensasiya edə bilər və Andersen sindromunda əzələ membranı potensialının azalmasının qarşısını alır. Əzələ parezinin hipokalemik formaları olan xəstələr şəkərsiz məhlulda həll edilmiş kalium xlorid qəbul edə bilərlər (adətən simptomlar bir saat ərzində yox olur); karbohidratla zəngin qidalardan və həddindən artıq idmandan uzaq durmalıdırlar. Əzələ iflicinin hiperkalemik formaları olan xəstələr tez-tez karbohidratla zəngin, az kalium olan yeməklər yeyərək bu hücumların qarşısını ala bilərlər.
Beləliklə, ürək və dayaq-hərəkət sistemlərindən fenotipik təzahürlərin müxtəlif üsullarla birlikdə qeyri-adi birləşməsinə görə irsi kanalopatiyalar arasında unikal patologiyalardan biri olan Andersen sindromunun klinikası, diaqnostikası və müalicəsi ilə bağlı bu günə qədər ən dolğun icmalı təqdim etdik.
mexanizmi hələ də aydın olmayan dismorfogenezin obrazlı əlamətləri. Uzun və ya qısa QT intervalı sindromu kimi genetik cəhətdən müəyyən edilmiş xəstəliklərin yeni variantlarının kəşfi kimi, molekulyar genetika sahəsində əlavə tədqiqatlar Andersen sindromunun yeni formalarını müəyyən etməyə, mutasiyaların təsir mexanizmlərini daha dərindən öyrənməyə kömək edəcəkdir (mutasiyalar ion kanallarının və transmembran zülallarının funksiyalarını poza bilər) və onların müxtəlif səviyyələrində bir-biri ilə qarşılıqlı əlaqəsini izah etmirsə, insan bu xəstəliyin ən xarakterik xüsusiyyətlərini izah etmir. farmakogenetik tədqiqatlar yeni müalicə üsullarının işlənib hazırlanmasına kömək edəcəkdir.
ƏDƏBİYYAT
1. Andersen E. D., Krasilnikoff P. A., Overad H. Fasiləli əzələ zəifliyi, ekstrasistollar və çoxsaylı inkişaf anomaliyaları: Yeni sindrom? // Acta Pediatr. Scand.
1971. - Cild. 60.-Səh.559-564.
2. Andelfinger G., Tapper A. R., Welch R. C. et al. KCNJ2 mutasiyası cinsə məxsus ürək və skelet əzələsi fenotipləri ilə Andersen sindromu ilə nəticələnir // Amer. J. Hum. Genet. - 2002. - Cild. 71.-Səh.663-668.
3. BakerN., Iannaccone S. T., BurnsD., Scott W. Andersen's syn-
drome: Epizodik zəiflik və ailə ventriküler disritmiya // J. Uşaq. Neyrol. - 1996. - Vl. 11. - S. 152 (Astr.).
4. Bendahhou S., Donaldson M. R., Plaster N. M. et al. qüsur-
tiv kalium kanalı Kir2.1 alveri Andersen-Tawil sindromunun əsasını təşkil edir // J. Biol. kimya. - 2003. - Cild. 278, No 51. - S. 51779-51785.
5. Bosch R. F., Li G. R., Gaspo R., Nattel S. Qvineya donuzunun ventrikulyar miyositlərinə tək və birlikdə xroniki amiodaron terapiyası və hipotiroidizmin elektrofizioloji təsiri // J. Pharmacol. Exp. Orada. - 1999. - Cild. 289. - S. 156-165.
6. Canun S., PerezN., Beirana L. G. Andersen sindromu üç nəsildə autosomal dominant // Amer. J. Med. Genet. - 1999. - Cild. 85. - S. 147-156.
7. Jen J., Ptacek L. J. Channelopathies // İrsi xəstəliyin metabolik və molekulyar əsasları / C. R. Scriver, A. L. Beaudet, W. S. Sly, D. Valle (eds). - N.Y.: McGraw-Hill, 2001.- S. 5223-5238.
ne və genetik olaraq təsdiqlənmiş ağır Andersen sindromunun müalicəsi üçün asetazolamid // Nevrologiya. - 2002.
Cild. 59, No 3. - S. 466.
9. Lange P. S., Er F., Gassanov N., Hoppe U. C. Andersen
KCNJ2 mutasiyaları yerli daxili rektifikatoru sıxışdırır
cari IK1 dominant-mənfi şəkildə // Kardiovasc. Res. - 2003. - Cild. 59, No 2. - S. 321-327.
10. Kimbrough J. et al. Uzun QT sindromu olan probandların təsirlənmiş valideynləri və bacıları üçün klinik təsirlər // Dövr. - 2001. - Cild. 104. - S. 557-562.
11. Klein R, Genelin R., Marks J. F. Kardiyak aritmiya ilə dövri iflic // J. Pediatr. - 1965. - Cild. 62. - S. 371-385.
12. Keating M. T., Sanguinetti M. C. Kardiyak aritmiyaların molekulyar və hüceyrə mexanizmləri // Hüceyrə. - 2001. - Cild. 104.
13. Levitt L. P., Rose L. I., Dawson D. M. Aritmiya ilə hipokalemik dövri iflic // N. Engl. J. Med. - 1972.
Cild. 286. - S. 253-254.
14. Plaster N. M. et al. Kir2.1-dəki mutasiyalar Andersen sindromunun inkişaf və epizodik elektrik fenotiplərinə səbəb olur // Hüceyrə. - 2001. - Cild. 105. - S. 511-519.
15. Pouget J., Philip N., Faugere G., Pellissier J. F. Andersen sindromu: Ürək ritminin pozulması ilə iflicin xüsusi bir forması // Rev. Neyrol. (Paris). - 2004. - Cild. 160, № 5 (2-ci bənd). - S. 38-42 (Fransız).
16 Sansone Ket başqa. Andersen sindromu: Fərqli dövri iflic // Ann. Neyrol. - 1997. - Cild. 42. - S. 305-312.
17. Schulze-Bahr E. Qısa QT sindromu və ya Andersen sindromu: Kir2.1 kanal disfunksiyasının Yin və yang // Circ. Res. - 2005. - Cild. 96. - S. 703-704.
18. Surawicz B. U dalğası: Faktlar, fərziyyələr, yanlış fikirlər və yanlış adlar // J. Cardiovasc. Elektrofiziol. - 1998.
Cild. 9. - S. 1117-1128.
19. Tawil R. et al. Andersen sindromu: kalium həssas dövri iflic, mədəcik ektopiyası və dismorfik xüsusiyyətlər // Ann. Neyrol. - 1994. - Cild. 35. - S. 326-330.
20. Tawil R. et al. Dövri ifliclərdə diklorfenamidin təsadüfi sınaqları. Dövri İflic üzrə İşçi Qrup // Yenə orada. - 2000. - Cild. 47. - S. 46-53.
21. Tricarico D., Barbieri M., Conte Camerino D. Acetazolamide əzələ KCa2+ kanalını açır: Dərmanın hipokalemik dövri iflicdə terapevtik təsirini izah edə bilən yeni fəaliyyət mexanizmi // Yenə orada. - 2000. - Cild. 48.
22. Tristani-Firouzi M., Jensen J. L., Donaldson M. R. et al. LQT7 (Andersen sindromu) ilə əlaqəli KCNJ2 mutasiyalarının funksional və klinik xarakteristikası // J. Clin. İnvestisiya edin. - 2002. - Cild. 110, No 3. - S. 381-388.
UDC 616.124.3:616.127]-07-08
AUTOSODOMINANT ARITMOGENİK KARDİOMİOPATİYA/SAĞ mədəciyin displaziyasının diaqnostikası, kursu və müalicəsi
L. A Bokeria, V. A Bazaev, A X. Melikulov, U. T. Kabaev, O. L. Bokeria, R. V. Viskov,
A G. Filatov, A N. Gritsai, V. V. Çumakov
Ürək-damar Cərrahiyyəsi Elmi Mərkəzi. A. N. Bakuleva (direktor - Rusiya Tibb Elmləri Akademiyasının akademiki L. A. Bokeriya) RAMS, Moskva
ritmogen sağ mədəciyin displaziyası və ya aritmogen sağ mədəciyin kardiomiopatiyası/displaziyası - qeyri-müəyyən etiologiyalı, çox vaxt irsi xarakter daşıyan patologiya
Miokardın, əsasən mədəaltı vəzinin ritmik və ya fibro-yağ infiltrasiyası, mədəciklərin fibrilasiyası da daxil olmaqla, müxtəlif şiddətdə mədəcik aritmiyaları ilə müşayiət olunur.
ARHİTMOLOGİYA SALNALARI, №4, 2005-ci il
Çoxsistemli kanalopatiyalar qrupundan olan nadir irsi xəstəlik. Varislik üsulu otosomal dominantdır, natamam transqressiya və eyni ailənin üzvləri arasında əhəmiyyətli dəyişkənlik var. Sporadik hallar nadir deyil. Qüsurlu gen (KCNJ2) 17-ci xromosomun uzun qolunda yerləşir (lokus 17q23.1-q24.2). Gen məhsulu kaliumun əzələ hüceyrələrinə daxil olduğu kalium kanallarının formalaşmasında iştirak edir. Gen mutasiyaya uğradıqda kalium kanallarının strukturu pozulur, eyni zamanda kalium ionlarının hüceyrəyə daxil olmasının tənzimlənməsi pozulur (tənzimləyici molekul PIP2 kanala bağlana bilmir). Kalium ionlarının əzələ hüceyrələrinə daxil olmasının pozulması sindromun xarakterik əlamətlərinin inkişafına səbəb olur (skelet sisteminin formalaşmasında KCNJ2 geninin rolu hələ də öyrənilir). Klinik olaraq sindrom əlamətlər triadası ilə təmsil olunur:
üzün və skeletin xarakterik dismorfizmi;
kalium-həssas dövri iflic;
mədəcik artemiyası.
Ürəyin qapaq aparatının zədələnməsi, böyrəklərin hipoplaziyası da mümkündür.
Displastik əlamətlər boy qısalığı, qulaqcıqların aşağı salınması, hipertelorizm, yumşaq və sərt damaq defektləri, mandibulyar hipoplaziya, klinodaktiliya və skoliozla təmsil olunur.
Andersen-Tavila sindromlu xəstənin üzü. Xarakterik displastik xüsusiyyətlərə diqqət yetirilir: hipertelorizm, aşağı çənənin hipoplaziyası və aşağı qurulmuş aurikullar. (mənbə Katz J.S., Wolfe G.I., Iannaccone S., Bryan W.W., Barohn R.J. Andersen sindromunda məşq testi // Arch. Neurol., 1999. - Vol.56. - S.352-356)
Bu sindrom üçün xarakterik olan miotonik təzahürləri olmayan kalium həssas dövri iflic hiperkalemik dövri iflicin digər formalarından klinik cəhətdən fərqlənmir. Bununla belə, belə bir fikir var ki, paralitik tutmalar zamanı kalium konsentrasiyasında düşmələrin həddindən artıq uyğunsuzluğu səbəbindən Andersen-Tavila sindromunda hipo-, normo- və hiperkalemik formalar üçün ənənəvi meyarlar qəbuledilməzdir. Çox vaxt nöbetlər uzun müddət davam edən ümumi zəiflik fonunda inkişaf edir.
Ürək simptomlarına müxtəlif şiddətdə Q-T intervalının uzadılması, mədəciklərin bigeminiyası, paroksismal ventrikulyar (biventrikulyar qədər) taxikardiya, qəfil ürək dayanması daxildir.
Ədəbiyyatda bu xəstəlikdən əziyyət çəkən xəstələrdə qəfil ölüm sindromu haqqında məlumatlar var.
Xəstələrdə tez-tez müxtəlif dərmanların qəbuluna paradoksal reaksiyalar və antiaritmik dərmanlara refrakterlik olur. Amiodaron və asetazolamid (diakarb) ilə terapiyanın davamlı müsbət təsiri göstərildi (ürək və əzələ simptomlarının dayandırılması).
İlk dəfə dövri iflic və aritmiyanın birləşməsini Klein et al. 1963-cü ildə ( Klein R., Ganelin R., Marks J.F., Usher P., Richards C. Kardiyak aritmiya ilə dövri iflic // J. Pediatr., 1963. - Vol.62. – S.371-385) və Lisak və b. 1970-ci ildə ( Lisak R.P., Lebeau J., Tucker S.H., Rowland L.P. Ürək aritmiya ilə hiperkalemik dövri iflic // Nevrologiya, 1970. - Vol.20. – S.386). Sindrom ilk dəfə 1971-ci ildə Danimarka həkimi Ellen Damgaard Andersen və başqaları tərəfindən təsvir edilmişdir. ( Andersen E. D., Krasilnikoff P. A., Overvad H. Fasiləli əzələli zəiflik, ekstrasistollar və çoxsaylı inkişaf etdirici anormallıqlar: a yeni sindromu? // Akta pediatriya Skandinaviya, Stokholm, 1971. – Cild.60. – P.559–564 ); o, xarakterik dövri iflic, aritmiya və inkişaf anomaliyaları olan 8 yaşlı uşağın vəziyyətini təsvir etdi. Sonradan belə bir triada 1985-ci ildə yalnız bir əsərdə təsvir edilmişdir. Və yalnız ətraflı təsviri, Livan mənşəli Amerikalı nevroloq, Rabbi Tawil et al. ( Tawil R., Ptacek L. J., Pavlakis S. G., DeVivo D. C., Penn A. S., Özdemir C., Griggs R. C. Andersen‘ s sindromu: kalium— həssas dövri iflic, mədəcik ektopiya, və dismorfik xüsusiyyətləri // İlnamələr of Nevrologiya, 1994. – Cild.35. – N.3. – P.326-330 ), mütəxəssislərin diqqətini bu nozoloji formaya cəlb edərək, onun sonrakı öyrənilməsini stimullaşdırdı.
Andersen xəstəliyi (IV tip qlikogenoz, amilopektinoz) 1,4-a-qlükan budaqlanan fermentin çatışmazlığı nəticəsində baş verir ki, bu da anormal, zəif həll olunan qlikogenin yığılmasına gətirib çıxarır.
Bu xəstəlik amilopektinoz adlanır, çünki belə hallarda qlikogen daha az budaqlanır və amilopektin quruluşu üçün xarakterik olan a-1,4-qlikozid bağlarını ehtiva edən daha uzun xətti bölgələrə malikdir.
Andersen xəstəliyi autosomal resessiv şəkildə miras alınır. 1,4-a-qlükan-şaxələnən ferment geni 3-cü xromosomda yerləşir; xəstəliyin əsasını təşkil edən onun mutasiyaları məlumdur və hər bir fərdi halda onların xarakteristikası xəstəliyin klinik mənzərəsini proqnozlaşdırmağa imkan verir.
Andersen xəstəliyinin simptomları
Amilopektinoz klinik cəhətdən heterojendir. Ən çox yayılmış klassik forma qaraciyərin mütərəqqi sirozu ilə xarakterizə olunur. İlkin əlamətlər - hepatosplenomeqaliya və zəif inkişaf - ilk 18 ayda görünür. həyat. Tədricən portal hipertenziya, assit, yemək borusunun varikoz damarları, qaraciyər çatışmazlığı inkişaf edir, xəstələr 5 yaşına qədər ölürlər. Nadir hallarda qaraciyərin zədələnməsi inkişaf etmir.
Andersen xəstəliyinin sinir-əzələ forması haqqında da məlumatlar var. Onun təzahürləri müxtəlifdir:
- ağır hipotansiyon, əzələ atrofiyası; doğum anından neyronların zədələnməsi; ölüm neonatal dövrdə baş verir;
- yaşlı uşaqlarda miyopatiya və miyokardın zədələnməsi;
Nömrələrdəki poliqojenane orqanlarının (sözdə poliglucosane bədən xəstəliyi) toplanmış diaqnozu ilə müşayiət olunan mərkəzi, periferik sinir sisteminə yayılma ziyanı, sonuncu vəziyyətdə diaqnozu, bu hüceyrələrlə məhdudlaşdığı üçün 1,4-a-Glucan-dallı fermentin fəaliyyətinin müəyyənləşdirilməsini tələb edir.
Andersen xəstəliyinin diaqnozu
Atipik qlikogen çöküntüsü qaraciyərdə, ürəkdə, əzələlərdə, dəridə, bağırsaqlarda, beyin və onurğa beynində və periferik sinirlərdə olur. Qaraciyərdə kiçik düyünlü siroz inkişaf edir. Hepatositləri tədqiq edərkən, amilazaya qismən davamlı, qaba dənəli PAS-müsbət çöküntülər olan zəif ləkələnmiş bazofil daxilolmalar görünür. Elektron mikroskopiya glikogen hissəciklərindən əlavə, amilopektin üçün xarakterik olan lifli aqreqatları aşkar edir. Sitoplazma daxilolmalarının xarakterik boyanması və elektron mikroskopik şəkil diaqnostik əhəmiyyətə malik ola bilərdi, lakin oxşar histoloji əlamətlər 1,4-a-qlükan-şaxələnən fermentin çatışmazlığı olmadan polisaxaridozlarda müşahidə edildi. Diaqnozu təsdiqləmək üçün qaraciyərdə, əzələlərdə, dəri fibroblastlarının mədəniyyətində və ya leykositlərdə bu xüsusi fermentin çatışmazlığını təyin etmək lazımdır. Prenatal diaqnostika məqsədi ilə kultivasiya edilmiş amniositlərdə və ya xorionik villilərdə 1,4-a-qlükan-şaxələnən fermentin aktivliyi müəyyən edilir.
Oxşar məqalələr